

总访问量:



王思杰,April 1, 2022
成岩重晶石的Ba同位素研究
—以塔里木盆地玉尔吐斯组为例
海洋输出生产力是碳循环的重要组成部分,准确测量地质历史时期的海洋输出生产力,对我们理解气候环境演变以及预测未来气候具有重要意义。由于生物重晶石(BaSO4)的形成与有机质再矿化相关,沉积物中生物重晶石的累积速率及其Ba同位素组成与有机碳输出通量呈正相关关系,因此生物重晶石的累积速率和其Ba同位素组成被认为是重建古海洋输出生产力的有力指标(Ma et al., 2014)。然而,生物重晶石在沉积成岩过程中,常会发生溶解以及再沉淀,其形态、S同位素、放射成因Sr同位素组成等均会发生显著改变(Paytan et al., 2002)。目前并不清楚在成岩作用过程中,生物重晶石的Ba同位素是否会发生改造。因此,本论文选用早寒武世塔里木盆地成岩重晶石来探讨成岩作用对生物重晶石Ba同位素的影响。
本工作的成岩重晶石采自塔里木盆地西北缘阿克苏地区,样品分别来自磷矿沟、肖尔布拉克、蓬莱坝、阿克苏四个剖面。在早寒武纪早期,该地区位于南天山洋的南缘,经历了裂谷、沉降和大规模海侵运动,广泛沉积了玉尔吐斯组层状硅质岩和黑色页岩。成岩重晶石赋存于黑色页岩中,呈结核状和条带状构造,镜下呈现树枝状、放射状结构,指示早期成岩作用的特征。
重晶石的沉淀主要受富硫酸盐流体和富钡流体的相互作用控制(Hanor, 2000),因此查清硫酸根和钡离子的来源是理解重晶石成因的必要前提。成岩重晶石δ34S变化范围较大,约为56.8‰ ~ 76.4‰ (Zhou et al., 2015),显著高于同期海水(35‰,Goldberg et al., 2005),表明成岩重晶石的硫酸盐经历了显著的瑞利分馏过程,应来自于硫酸盐细菌还原作用后的残余在孔隙水中的硫酸根。成岩重晶石δ138/134Ba变化范围较大,为-0.15‰ ~ +0.51‰,平均值为0.17 ± 0.29‰ (n=21),且与87Sr/86Sr呈正相关关系(R2=0.32),与δ34S没有相关性(R2=0.0005)(如图1所示)。这表明成岩重晶石的Ba与Sr的来源较为相似,而与S发生的氧化还原过程无关。成岩重晶石样品的87Sr/86Sr比值为0.7083~0.7090,大部分样品的87Sr/86Sr比值显著高于同期海水(0.7082~0.7086;Li et al., 2013),而只有小部分样品的87Sr/86Sr比值与同时期海水一致,这表明成岩重晶石的Sr遭受了海洋沉积物中的硅质碎屑的改造 (87Sr/86Sr约为0.720, Faure and Powell., 2012)。根据87Sr/86Sr与δ138/134Ba
 |
的相关性,我们认为成岩重晶石Ba同位素组成可能也遭受海洋沉积物的改造。
图1
由于生物重晶石沉淀带走海水中的轻Ba同位素以及表现出与海水一致的87Sr/86Sr比值 (δ138/134Ba变化范围为-0.21‰~+0.13‰ (n=114),Horner et al., 2017;Crockford et al., 2019),因此原生生物重晶石溶解可以为成岩重晶石提供轻Ba同位素组成、低87Sr/86Sr比值的Ba和Sr源。早寒武世牛蹄塘组黑色页岩的δ138/134Ba可达1.09 ± 0.01‰,Ba含量可高达10000 μg/g (Dong et al., under review),同时期的沉积物中硅质碎屑具有高87Sr/86Sr比值。因此,外来流体(热液或者平流孔隙水)淋滤早寒武世的沉积物时,能为玉尔吐斯组成岩重晶石高87Sr/86Sr比值和重δ138/134Ba的端元提供Ba和Sr源。
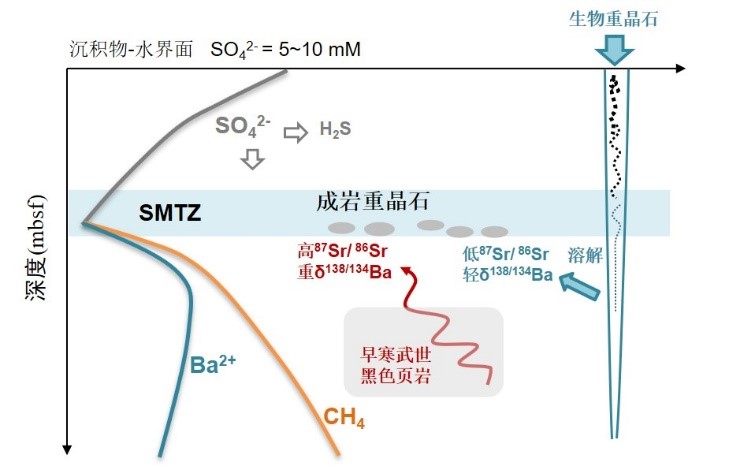
硫酸盐-甲烷转换带(SMTZ)是成岩重晶石沉淀的关键,在SMTZ上方是硫酸盐还原区,由于海水硫酸根对沉积物的补充,原生重晶石处于相对稳定的状态;在SMTZ下方是甲烷稳定区域,硫酸根与甲烷发生氧化还原反应促使生物重晶石溶解,形成富含原生重晶石特征的流体(低87Sr/86Sr比值和轻δ138/134Ba)。当外来流体淋滤周围沉积物,可能会形成高87Sr/86Sr比值和高δ138/134Ba的流体。当含硫酸根流体与富含Ba2+的流体在SMTZ区域相遇时,则沉淀形成成岩重晶石。因此,低87Sr/86Sr比值(与同时期海水一致)与低δ138/134Ba的重晶石代表原生重晶石,高87Sr/86Sr比值(高于同时期海水)与高δ138/134Ba的重晶石为受到成岩作用改造的重晶石。此外,在使用重晶石Ba同位素反演古海洋生产力之前,需要严格排除成岩作用对Ba同位素的影响,并确定能代表生物重晶石的Ba同位素组成。
参考文献
Ma, Z., Gray, E., Thomas, E., Murphy, B., Zachos, J. and Paytan, A., 2014. Carbon sequestration during the Palaeocene–Eocene Thermal Maximum by an efficient biological pump[J]. Nature Geoscience 7(5), 382-388.
Paytan, A., Mearon, S., Cobb, K. and Kastner, M., 2002. Origin of marine barite deposits: Sr and S isotope characterization[J]. Geology 30(8), 747-750.
Hanor, J.S., 2000. Barite–celestine geochemistry and environments of formation[J]. Reviews in Mineralogy and Geochemistry 40(1), 193-275.
Zhou, X., Chen, D., Dong, S., Zhang, Y., Guo, Z., Wei, H. and Yu, H., 2015. Diagenetic barite deposits in the Yurtus Formation in Tarim Basin, NW China: Implications for barium and sulfur cycling in the earliest Cambrian[J]. Precambrian Research 263, 79-87.
Goldberg, T., Poulton, S.W. and Strauss, H., 2005. Sulphur and oxygen isotope signatures of late Neoproterozoic to early Cambrian sulphate, Yangtze Platform, China: diagenetic constraints and seawater evolution[J]. Precambrian Research 137(3-4), 223-241.
Li, D., Ling, H.-F., Shields-Zhou, G.A., Chen, X., Cremonese, L., Och, L., Thirlwall, M. and Manning, C.J., 2013. Carbon and strontium isotope evolution of seawater across the Ediacaran–Cambrian transition: Evidence from the Xiaotan section, NE Yunnan, South China[J]. Precambrian Research 225, 128-147.
Faure, G., and Powell, J. L. Strontium isotope geology (Vol. 5)[M]. Springer Science & Business Media, 2012.
Horner, T.J., Pryer, H.V., Nielsen, S.G., Crockford, P.W., Gauglitz, J.M., Wing, B.A. and Ricketts, R.D., 2017. Pelagic barite precipitation at micromolar ambient sulfate[J]. Nature Communications 8(1), 1-11.
Crockford, P.W., Wing, B.A., Paytan, A., Hodgskiss, M.S.W., Mayfield, K.K., Hayles, J.A., Middleton, J.E., Ahm, A.-S.C., Johnston, D.T., Caxito, F., Uhlein, G., Halverson, G.P., Eickmann, B., Torres, M. and Horner, T.J., 2019. Barium-isotopic constraints on the origin of post-Marinoan barites[J]. Earth and Planetary Science Letters 519, 234-244.
Dong et al., under review.
你必须登录之后才可以参与讨论。