

总访问量:


孙楠,Feb. 10, 2022
01 为什么研究重晶石?
重晶石是一种常见的、化学性质高度稳定的矿物,能在海洋和大陆的多种环境下存在。在氧化环境中,重晶石具有成岩稳定性,早期成岩作用中海洋重晶石保存率可达30%。在前人的研究中,海洋重晶石是海洋初级生产力的重要指示物,其O、S以及放射成因Sr同位素(δ34S,δ18O, 87Sr/86Sr)也在记录海水同位素组成和指示重晶石沉淀溶液的来源中有重要应用。
随着分析技术的发展,高精度的 Ba同位素(δ138/134Ba)和稳定Sr同位素(δ88Sr)在地球化学领域获得了越来越多的关注。重晶石是Ba的主要矿物之一,也是记录Sr同位素的重要工具。重晶石的Ba同位素数据为古环境的研究提供了新的手段,对制约海洋环境变化以及全球Ba循环有重要意义。稳定成因Sr同位素也可用于纪录海水同位素组成变化与制约海洋碳循环,以及理解沉积后和成岩过程。因此,对重晶石中的Ba和Sr进行同位素分析有着重要的地质意义。
由于重晶石在水和无机酸中超低的溶解度(Ksp=10-9.96),样品消解是这类样品进行同位素测试时最大的难点。目前主要的消解方法有:碳酸钠置换法,络合法,HI 溶解法和水提取法。其中,碳酸钠置换法流程相对便捷并且安全,可以获得足量的Sr进行分析。中科大金属稳定同位素实验室基于前人的研究,开发了同时适用于重晶石的Ba和稳定Sr同位素分析的碳酸钠置换法,并检验了该方法的可靠性。
02 关键的化学流程
碳酸钠置换法最早在1985年由Breit提出并用于放射成因Sr同位素分析,其主要原理是用过量的CO32-置换SO42-从而形成可溶的碳酸盐:
(Ba,Sr)SO4(s)+ CO32- (aq) → BaCO3(s)+ SrCO3(s)+ SO42- (aq)
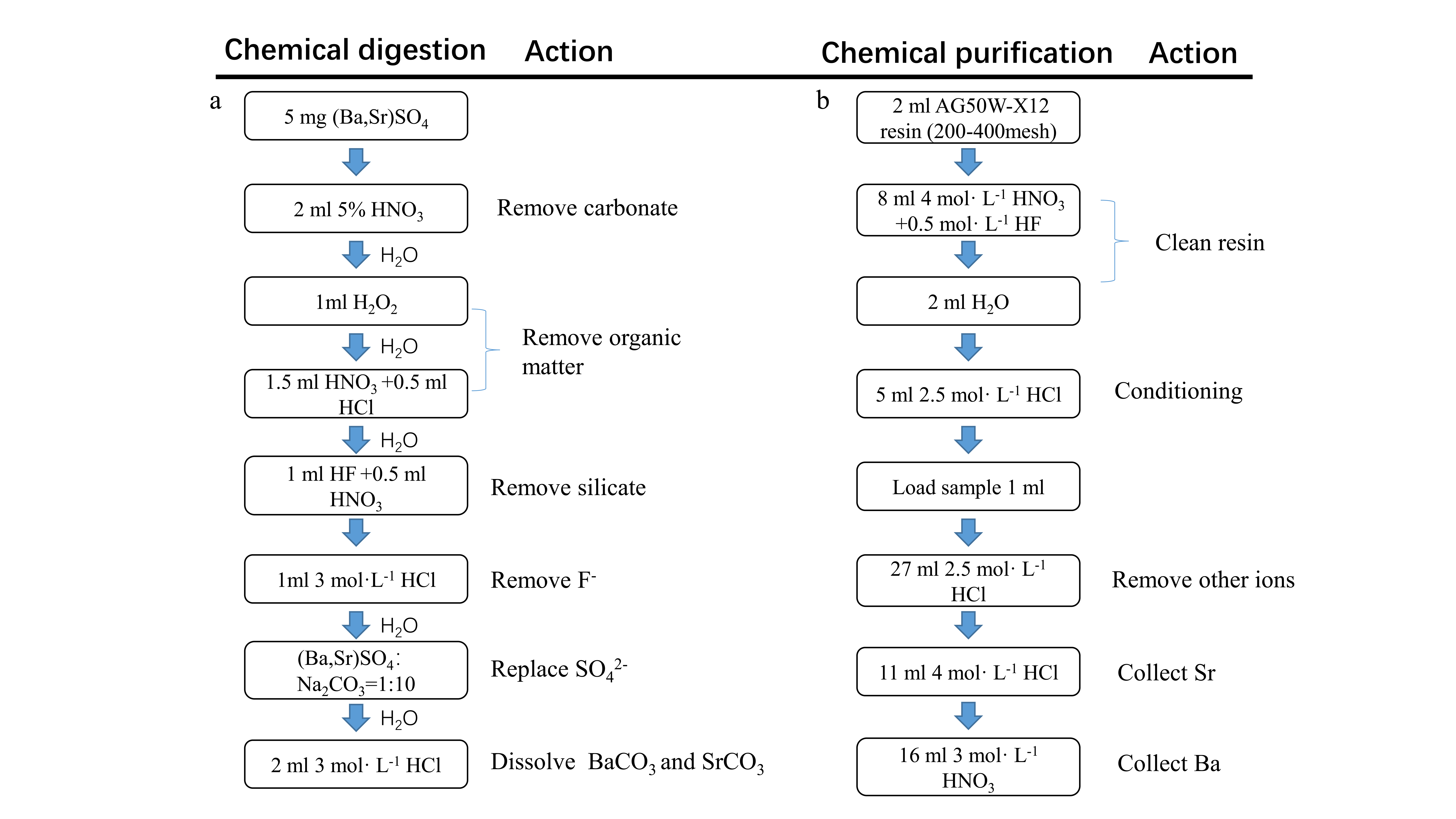
首先我们通过酸和双氧水去除杂质,得到纯净的重晶石,之后通过置换反应,将重晶石中的Ba2+ 、Sr2+及其他常见的阳离子(如Pb2+,Ca2+等)富集于固相碳酸盐中(图1a,化学消解流程),再进行化学纯化。
图1 碳酸钠置换法化学流程
化学纯化流程如图1b所示。在这个过程中我们发现,在接取Sr后继续添加HNO3,Ba也会被洗脱出来,并且能与其它元素很好地分离(图2)。这使得我们实现了重晶石Ba、Sr的一柱分离。
图2 重晶石Ba、Sr淋滤曲线
03 精确度和准确性
双稀释剂法能够有效校正单次测量的仪器分馏,其在多接收电感耦合等离子体质谱仪(MC-ICP-MS)上的应用,极大地提高了我们的分析精度。在Ba同位素分析中,我们选取135Ba–136Ba作为双稀释剂,长期外部精度δ137/134Ba优于0.05‰ (2SD)。在稳定Sr同位素分析中,我们选取84Sr-87Sr作为双稀释剂,分析精度可达0.03‰ (2SD)。
在建立方法的过程中,我们通过合成标准溶液和合成重晶石等方法进行对比实验,严格检验了基质效应以及置换过程是否产生同位素分馏的问题。结果表明,我们测得的纯重晶石国际标样(NBS127)δ138/134Ba值与前人一致,化学消解流程也可以很好地去除杂质。值得注意的是,当置换不完全时(重晶石没有完全转换为碳酸盐)会发生较小的稳定Sr同位素δ88Sr分馏(~0.4‰),因此,在进行稳定Sr同位素分析时我们需要保证重晶石被完全置换。
04 报道的标样数据
基于上述方法,我们首次报道了中国的五个天然重晶石标准样品的Ba同位素和稳定Sr同位素值(图3,图4)。
图3 重晶石标准样品δ137/134Ba组成
图4重晶石标准样品的δ88Sr和87Sr/86Sr组成
将来,我们可以利用此方法测量自然重晶石样品的Ba和Sr同位素,研究地质历史时期全球海洋演化等过程。
论文信息:
【1】L.-L. Tian, Z. Zeng, X.-Y. Nan, H.-M. Yu, F. Huang, Determining Ba isotopes of barite using the Na2CO3 exchange reaction and double-spike method by MC-ICP-MS. Journal of Analytical Atomic Spectrometry 34, 1459-1467 (2019).
【2】N. Sun, X.-Q. Chen, L.-L. Tian, F. Huang, Determining 88Sr/86Sr of barite using
the Na2CO3 exchange method. Journal of Analytical Atomic Spectrometry, 37, 390-398 (2022).